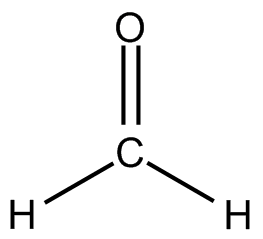
Формула формальдегида
Формальдегид - это газ с едким запахом. Он химически очень активен (что и объясняет его запах и раздражающие свойства) и довольно токсичен. Тем не менее он широко применяется для дезинфекции и консервации (в очень небольших количествах, порядка долей процента и, конечно же, не для пищевых продуктов). Основное и самое известное его применение - для дезинфицирующих растворов в виде раствора в воде под названием "формалин".
Слово "альдегид" - это сокращение от "спирт, лишённый водорода". И правда, формула формальдегида отличается от формулы метанола на молекулу водорода. При определённых условиях можно осуществить дегидрирование метанола (и других спиртов), но основной способ получения формальдегида - окисление метанола, при этом водород превращается в воду. На этом основан и качественный тест на метанол - если опустить раскалённую медную проволочку в метанол, появится неприятный запах формальдегида. При этом окислителем является оксид меди, который в небольшом количестве образуется на поверхности меди. Если же спирт этиловый, то при окислении образуется ацетальдегид, по запаху напоминающий яблоки.
Получать формальдегид в лаборатории нет никакого резона. Что касается других альдегидов, то они обычно получаются окислением соответствующих спиртов бихроматом калия, триокисью хрома или более изощрёнными реагентами. Сложность состоит в том, что альдегиды сами способны окисляться дальше, в соответствующие кислоты. Например, формальдегид окисляется в муравьиную кислоту (отсюда и название - муравьиная кислота по-английски "formic acid"), ацетальдегид - в уксусную кислоту. Здесь выбор реагентов уже гораздо богаче: и перманганат калия, азотная кислота, и избыток того же дихромата калия. Но наиболее интересными лабораторными реакциями являются реакции с оксидами меди и серебра.
Реакция "серебрянного зеркала" - это восстановление альдегидами аммиачного раствора оксида серебра, при этом выпадает металлическое серебро.
Альдегиды окисляются также свежеосаждённой гидрокисью меди, при этом образуется закись меди, имеющая красный цвет:
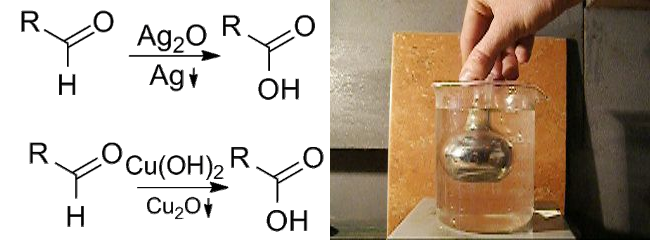
Окисление альдегидов. Справа – реакция серебряного зеркала.
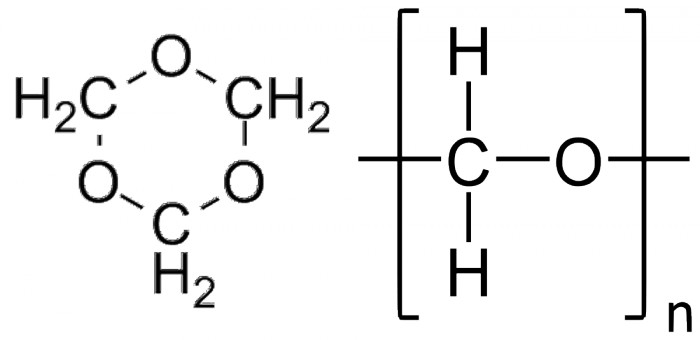
При длительном хранении из формалина - раствора формальдегида - выпадает белый желеподобный осадок. Это параформ - полимер формальдегида. При необходимости кипячением в сильной кислоте (например, серной) параформ можно деполимеризовать обратно. Вообще формальдегид образует несколько полимеров, начиная от триоксана (триоксиметилена) и заканчивая полиоксиметиленом (POM) - производящимся промышленно полимером с важными механическими свойстваим: низким коэффициентом трения и высокой износоустойчивостью. Также триоксан используется как компонент таблеток сухого горючего.
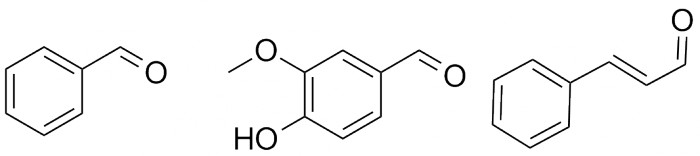
Высшие альдегиды гораздо менее токсичны - например, бензальдегид используется как ароматическая добавка, поскольку именно он придаёт маслу горького миндаля его характерный запах. Есть ещё два альдегида с легко узнаваемым запахом: это ванилин, являющийся производным бензальдегида, и циннамальдегид (коричный альдегид), содержащийся, как легко догадаться, в корице.
Альдегидами являются и некоторые сахара, например, глюкоза.
Реакции альдегидов: http://orgchem.ru/chem4/link_v3451.htm
Полиоксиметилен: https://en.wikipedia.org/wiki/Polyoxymethylene
Фотогрфия реакции «серебряного зеркала» взята с сайта http://chemistry-chemists.com