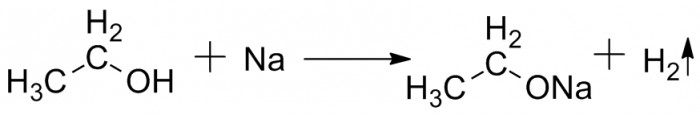
В первую очередь спирты в некотором отношении родственны воде, т.к. так же, как и вода, содержат OH- группу. Поэтому спирты реагируют с щелочными металлами с выделением водорода и образованием соединения, называющимся алкоголятом. Для метилового спирта оно будет называться метилатом, для этилового - этилатом, и так далее.
Реакция идёт обычно более спокойно, чем с водой (собственно, так и рекомендуют уничтожать остатки натрия или калия – заливая их спиртом), и алкоголяты являются более сильными основаниями, чем гидроксиды. Поэтому при добавлении воды (или при её наличии в спирте изначально) произойдёт реакция обмена с образованием соответствующего гидроксида и исходного спирта. В некоторых случаях эта реакция используется для осушения спиртов.
Алкоголяты щелочных металлов используются в органической химии как катализаторы или сильные основания (рекордсмен - трет-бутилат калия). Изопропилат алюминия является восстановителем.
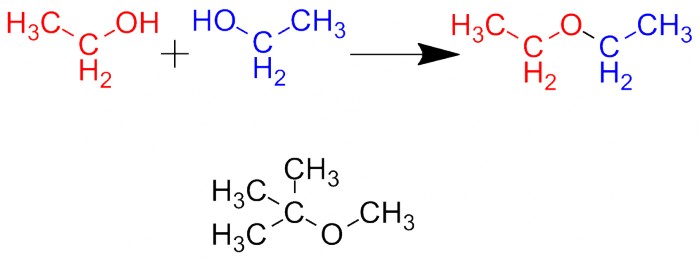
Под действием кислоты и/или водоотнимающих реагентов две молекулы спирта могут соединиться с выделением молекулы воды. Получится вещество, имеющее кислородный "мостик". Такие вещества называются эфирами. Например, из этилового спирта получается диэтиловый эфир (это тот, который называют просто "эфиром"). Эфиры испаряются легче, чем соответствующие спирты, и очень хорошо горят - поэтому диэтиловый эфир используется в смесях для запуска двигателей на морозе, а метил-трет-бутиловый эфир используется как присадка к бензину, повышающая его октановое число.
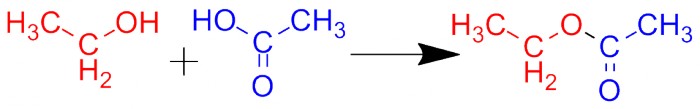
Карбоновые кислоты тоже имеют ОН-группу, и аналогичная реакция может пройти между кислотой и спиртом. При этом образуется соединение, называющееся сложным эфиром. Изображённое на рисунке вещество называется этиловым эфиром уксусной кислоты. Все другие сложные эфиры именуются аналогично, но иногда такие называния сокращают, используя названия фрагмента кислоты: например, этилацетат.
Сложные эфиры в небольших концентрациях пахнут приятно - запах напоминает запах фруктов. Это и неудивительно, поскольку это и есть те самые вещества, которыми и пахнут фрукты. Например, этиловый эфир масляной кислоты пахнет ананасами, амиловый эфир уксусной кислоты пахнет бананами, а этиловый эфир гептановой кислоты пахнет виноградом. Считается, что этилацетат тоже пахнет фруктами, но большинство людей скажет, что его запах - это запах лака для ногтей. Всё это нетрудно проверить - реакция получения сложных эфиров описана в любом лабораторном практикуме и легко воспроизводится даже людьми, не имеющими большого опыта в синтезе.
Жиры являются сложными эфирами глицерина и т.н. "жирных" (содержащих 12-20 атомов углерода) карбоновых кислот.
В жёстких условиях (например, нагревание с концентрированной серной кислотой) спирты могут дегидратироваться с отщеплением молекулы воды и образованием ненасыщенного (содержащего двойную связь) соединения. Этанол дегидратируется в этилен, изопропанол - в пропилен. Третичные спирты дегидратируются проще всего - под действием каталитических количеств любой сильной кислоты.
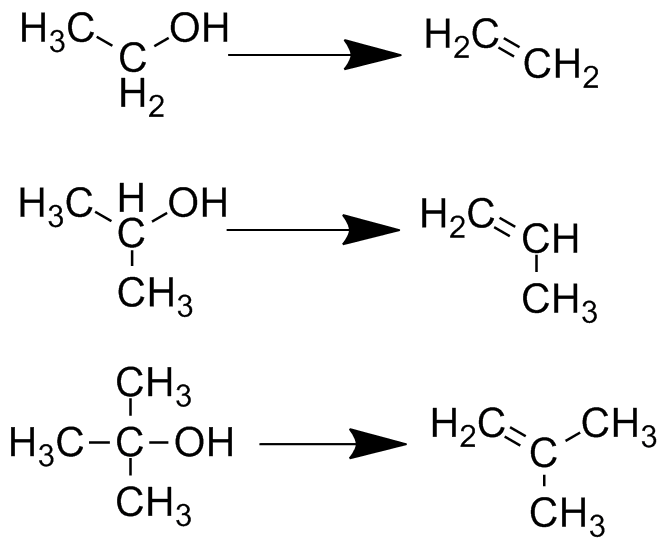
Реакция дегидратации спиртов
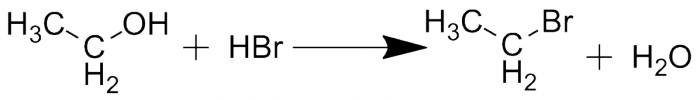
Под действием, например, бромоводорода ОН-группа может отщепиться и на её место встанет атом брома. Реакция обратима (так же, как и реакция этерификации) и представляет собой способ получения алкилбромидов. Поскольку все вышеописанные реакции (образование простого эфира, дегидратация и замена гидроксильной группы на галоген) проходят в сходных условиях, все они являются конкурирующими и ответственны за образование побочных продуктов.
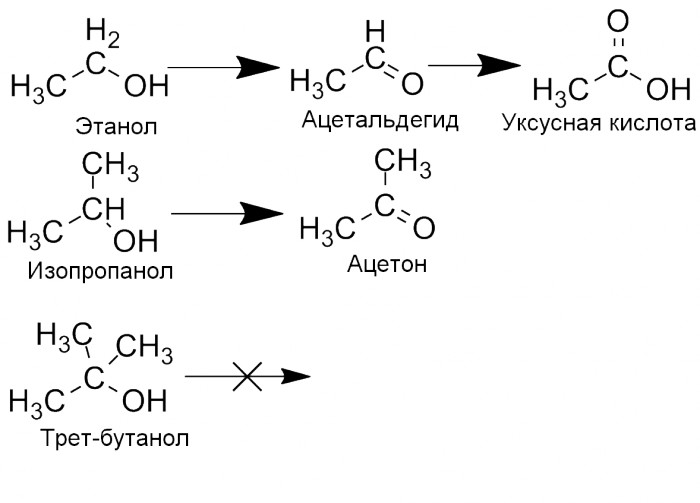
Спирты также способны окисляться. В случае с первичными спиртами продуктом будет альдегид и соответствующая карбоновая кислота. Вторичные спирты не могут образовывать кислоты (вернее, могут, но в жёстких условиях и с разрывом C-C связи), поэтому реакция останавливается на веществе, которое называется кетоном. Простейший пример - это ацетон (диметилкетон), получающийся окислением изопропанола. Третичные спирты окисляться не способны.
Окислителем может являться, например, перманганат калия (марганцовка), дихромат калия или триоксид хрома, двуокись марганца, а также кислород воздуха. Также окисление спиртов способны производить аэробные бактерии, получающие при этом энергию. В организме этанол превращается ферментами печени сначала в ацетальдегид (который токсичен), а затем в уксусную кислоту (нетоксичную в разумных количествах).
Применения изопропилата натрия: https://www.alfa.com/ru/catalog/089446/
Восстановление изопропилатом алюминия называется восстановлением по Меервейну-Понндорфу-Верли (Meerwein–Ponndorf–Verley reduction). Пример можно найти, например, в книге «Лабораторные работы в органическом практикуме» Агрономова, с.131 и 133.
Методику получения сложных эфиров можно найти в том же Агрономове (стр. 78)