Начнём, как обычно, с неорганического соединения - сероводорода H2S. Это газ (в отличие от H2O, несмотря на то, что сера тяжелее кислорода), вредный и неприятно пахнущий. Говорят, что сероводород пахнет тухлыми яйцами, хотя вернее будет то, что тухлые яйца пахнут сероводородом - он образуется в процессе гниения. Это означает, что сера содержится в живых организмах в виде каких-то соединений. Но обо всём по порядку.
Если заменить один из водородов в сероводороде на метильный радикал, то получится соединение, называемое метилмеркаптаном. Используя другие радикалы, мы получим ряд меркаптанов.
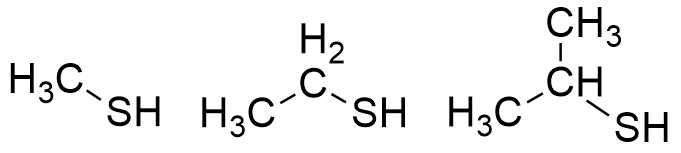
Меркаптаны
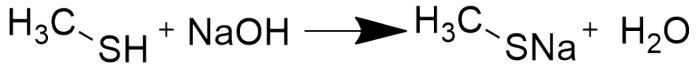
Поскольку сера находится в той же группе, что и кислород, то и меркаптаны по свойствам должны быть подобны спиртам. Однако сера гораздо слабее участвует в водородной связи, поэтому низшие меркаптаны являются газами. Так же, как и спирты, меркаптаны являются кислотами, однако гораздо более сильными, и гораздо проще образуют соли с основаниями, образуя т.н тиоляты металлов.
Реакция меркаптанов с основаниями с образованием тиолятов
Подобно сероводороду, меркаптаны неприятно пахнут. Однако "неприятно" - это слабо сказано. Этилмеркаптан добавляют к природному газу (поэтому все и так знают, как пахнут меркаптаны), но запах ощущается уже в концентрации 1 молекула меркаптана на 50 миллионов молекул воздуха! Скунсы выделяют меркаптаны для защиты от хищников. Более тяжёлые меркаптаны менее летучи и поэтому не столь вонючи, однако по этой же причине запах может не выветриваться с одежды неделями.
Если в сероводороде заменить оба атома водорода на алкильные радикалы, то получится соединение, аналогичное эфиру - тиоэфир. В целом по свойствам они похожи на эфиры, если вы решитесь когда-нибудь связаться с ними... Да, они воняют так же, как и меркаптаны, Однако есть и отличие в химических свойствах. Вообще сернистые соединения (хоть и более сложные) обуславливают запах жареного лука, чеснока, хрена и дуриана.
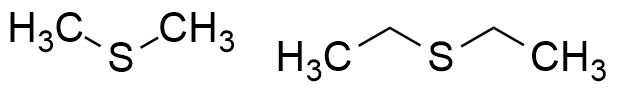
Простейшие тиоэфиры – диметилсульфид и диэтилсульфид
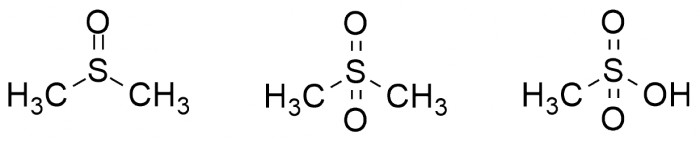
Сера способна принимать разные степени окисления, вплоть до +6 (в отличие от кислорода). Поэтому меркаптаны и тиоэфиры, соответствующие степени окисления -2, могут окисляться дальше, образуя сульфоксиды, сульфоны и сульфоновые кислоты. Существуют также т.н. сульфиновые кислоты, но они неустойчивы и встречаются редко.
Диметилсульфоксид, диметилсульфон, метансульфоновая кислота
Диметилсульфоксид - очень интересное соединение. Он практически безвреден для организма, растворяет многие неорганические соединения (аналогично воде), неограниченно смешивается с водой. Поэтому его используют как компонент лекарственных мазей, а также в процессе криоконсервации. Я уже писал про то, что ДМСО - ценный и часто используемый растворитель в синтезе. Да, он, как и все окисленные соединения серы, не пахнет, за исключением всегда присутствующей примеси диметилсульфида.
Диметилсульфон соответствует высшей степени окисления серы. Интересно, что он встречается в атмосфере, и некоторые бактерии, живущие в воздухе (!) на высоте 7-10км (!), используют его как источник углерода. Да, надо сказать, что в тех местах, где с кислородом туго (например, на дне океанов), бактерии используют соединения серы для получения энергии. Сероводорода и серной кислоты полно в продуктах извержения вулканов.
Сульфокислоты можно считать аналогами серной кислоты, которые, в отличие от последней, легко растворяются в органических растворителях. Наиболее часто используемые - это метансульфокислота и толуолсульфокислота и различные их производные. Толуолсульфокислота, кстати, является побочным продуктом производства сахарина.
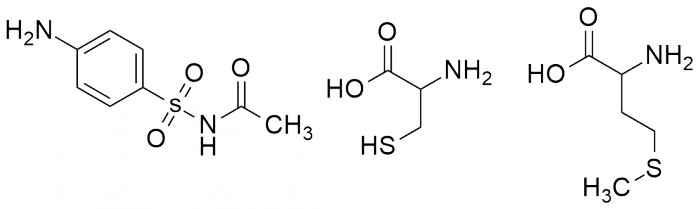
В целом, многие лекарственные или природные соединения содержат серу в своей молекуле. Говоря о сульфокислотах, стоит упомянуть, что они, подобно карбоновым кислотам, образуют амиды, называемые сульфамидами. Производные сульфамида были одними из первых открытых человеком антибиотиков. Пенициллин, открытый позднее, тоже, кстати, содержит серу в своей структуре.
Сульфаниламид – представитель сульфамидов. Цистеин и метионин.
Аминокислота цистеин является также и меркаптаном, а метионин - тиоэфиром, и неспроста. Метионин принимает непосредственное участие в биосинтезе многих важных соединений в организме, а цистеин содержится в белках шерсти и ногтей (кератине), придавая им прочность. Это достигается образованием т.н. дисульфидных связей (связей –S-S–), которые связывают между собой разные части молекулы белка, а иногда и разные молекулы между собой. Химическая завивка волос заключается в разрыве этих связей и образовании их заново, так что форма волоса меняется уже практически необратимо.
Кстати, вулканизация резины – в чём-то похожий процесс: при нём различные молекулы каучука «сшиваются» между собой посредством дисульфидных и трисульфидных мостиков. Это придаёт продукту прочность и жёсткость.
Бактерии, питающиеся диметилсульфоном: http://www.pnas.org/content/110/7/2575.full.pdf
Сахарин https://ru.wikipedia.org/wiki/Сахарин
О запахе дуриана https://lenta.ru/news/2017/01/20/durian/
Вулканизация (см. картинку справа) https://ru.wikipedia.org/wiki/Вулканизация