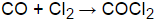2. Змішали однакові об'єми чадного газу і хлору. Початковий тиск у посудині складав 2 атм.Яким став тиск після того,коли прореагувало 75% чадного газу?
3.Через розчин станум(ІІ)хлориду протягом 1 години пропускали постійний електричний струм силою 2,68А. На катоді виділилось 5,93 г олова.Визначити евівалент стануму в його солі.Який об'єм газу (і якого?) виділився на аноді? еквівалент я найшов