Процес втрати частинкою електрону називається окисненням, а процес приєднання електронів - відновленням. У реакціях ці два процеси протікають одночасно - одні частинки окиснюються, інші відновлюються.
Речовини, які приєднують електрони, називаються окисниками, а речовини, які втрачають електрон - відновниками. В даному прикладі:
Cu2+ + 2e- = Cu
Zn - 2e- = Zn2+
Cu2+ - окисник, Zn - відновник, тобто мідь знижує ступінь окиснення, цинк - збільшує.
Рівняння окисно-відновних реакцій
Використовують два методи складання рівнянь для реакції окиснення-відновлення. Один метод базується на використанні ступенів окиснення. Підвищення ступені окиснення у одного елемента та її зниження у іншого відбувається одночасно. Так, при взаємодії алюмінію та сірки:
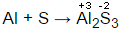
Ступінь окиснення алюмінію збільшується на 3 одиниці
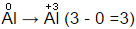
а ступінь окиснення сірки знижується на 2 одиниці
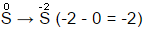
Щоб встановити коефіцієнти у рівнянні реакції, потрібно знайти кратне для чисел, що показують підвищення та зниження ступенів окиснення:
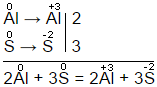
Отримані коефіцієнти переносяться у рівняння реакції:
Рівняння окисно-відновних реакцій
Використовують два методи складання рівнянь для реакції окиснення-відновлення. Один метод базується на використанні ступенів окиснення. Підвищення ступені окиснення у одного елемента та її зниження у іншого відбувається одночасно. Так, при взаємодії алюмінію та сірки:
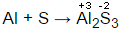
Ступінь окиснення алюмінію збільшується на 3 одиниці
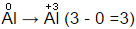
а ступінь окиснення сірки знижується на 2 одиниці
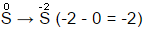
Щоб встановити коефіцієнти у рівнянні реакції, потрібно знайти кратне для чисел, що показують підвищення та зниження ступенів окиснення:
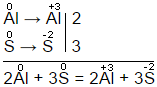
Отримані коефіцієнти переносяться у рівняння реакції:
Al + S = Al2S3
Іонно-електронний метод. Метод складання рівнянь окисно-відновних реакцій використовується для іонно окисно-відновних процесах та базується на складанні частинних рівнянь реакцій відновлення іонів (молекул) окисника та окиснення іонів (молекул) відновника з наступним сумуванням їх у спільне рівняння. Для цього необхідно скласти іонну схему реакції. Іони які не змінюються в результаті реакції у схему не включаються.
Список використаної літератури
- Загальна та неорганічна хімія: Підручник для студ. вищ. навч. закл. / О.М. Степаненко, Л. Г. Рейтер, В. М. Ледовських, С.В. Іванов. - К.: Пед. преса, 2000. - 784 с.: іл. ISBN 966-7320-13-8
- Ахметов Н.С. Общая и неорганическая химия. Учеб. для вузов. - 4-е изд., испр. - М.: Высш. шк., Изд. центр "Академия", 2001. - 743 с., ил.
