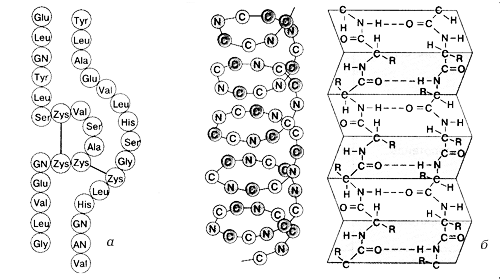
Функції білків організму дуже різноманітні. Білки-ферменти забезпечують протікання біохімічних реакцій і грають важливу роль в обміні речовин. Деякі білки виконують структурну або механічну функцію, утворюючи цитоскелет, що підтримує форму клітин. Також білки грають важливу роль в сигнальних системах клітин, при імунній відповіді і в клітинному циклі. У бодібілдингу основне значення надається скорочувальної функції протеїну - все довільні і мимовільні рухи виробляються за рахунок взаємодії білкових молекул.
| Амінокислота | Сироватковий альбумін | Сироватковий глобулін | Яєчний альбумін | Казеїн | Гістон тимуса | Інсулін |
| Аланін | - | - | 7,2 | 5,5 | - | - |
| Аргінін | 6,0 | 4,8 | 5,9 | 4,3 | 12,9 | 2,3 |
| Аспарагінова кислота | 9,9 | 8,8 | 8,1 | 6,1 | - | 6,8 |
| Валін | 7,0 | 9,8 | 6,8 | 6,5 | 4,4 | 8,8 |
| Гістидин | 3,5 | 2,5 | 1,7 | 2,1 | 3,0 | 5,3 |
| Гліцин | 2,0 | 4,2 | 3,2 | 0,5 | - | 4,6 |
| Глутамінова кислота | 17,1 | 11,8 | 17,5 | 23,3 | - | 2,1 |
| Ізолейцин | 2,0 | 3,1 | 7,1 | 6,3 | 6,0 | 2,9 |
| Лейцин | 11,9 | 7,9 | 10,0 | 9,7 | 7,4 | 14,0 |
| Лізин | 10,4 | 6,7 | 5,0 | 7,6 | 11,7 | 2,3 |
| Метіонін | 1,3 | 1,1 | 5,1 | 0,4 | 1,3 | 0,0 |
| Пролін | 7,8 | 8,1 | 4,5 | 7,9 | - | 2,9 |
| Серін | 3,7 | 11,4 | 7,4 | 7,7 | 3,8 | 3,5 |
| Тирозин | 5,3 | 6,8 | 4,3 | 6,7 | 4,4 | 12,7 |
| Треонін | 5,1 | 8,4 | 4,0 | 3,8 | 5,7 | 2,7 |
| Триптофан | 0,3 | 2,9 | 1,5 | 1,2 | 0,04 | 0,0 |
| Фенілаланін | 7,9 | 4,6 | 5,4 | 5,0 | - | 8,2 |
| Цистеїн | 6,5 | 3,1 | 1,9 | 0,35 | 0,5 | 12,7 |
Класифікація білків
Усі білки розділяють на дві великі групи: протеїни (інакше прості білки), в склад яких входять лише залишки амінокислот, та протеїди (або складні білки) - сполуки простого білку (протеїну) з речовиною небілкової природи. Протеїни та протеїди розділяються на ряд підгруп.
Протеїни:
| Протеїди:
|
Протеїн в бодібілдінгу
Враховуючи різноманіття функцій і біологічних ефектів протеїну та його складових - амінокислот, у бодібілдингу білки використовують в різних цілях: для зниження жирової маси тіла, для стимуляції росту м'язів, а також з метою підтримки здорової фізичної форми.
Вміст у продуктах харчування
Головним джерелом білків для людини є харчові продукти тваринного та рослинного походження. Головним чином тваринні (м'ясо, риба, сир) та тільки деякі рослинні (горох, соя) продукти багаті білками, у той час як найбільш поширені рослинні харчові продукти містять невелику кількість його.
Табл. Вміст білка у деяких харчових продуктів
Перевірка на справжність
Широко поширений простий спосіб перевірки білка на справжність шляхом додавання до нього окропу, іноді з подальшим кип'ятінням , внаслідок чого спостерігається процес денатурації з утворенням характерних пластівців і випаданням осаду. Для посилення реакції бажано додати кілька крапель оцту, щоб знизити pH розчину і нейтралізувати негативний заряд.
Деякі продукти не проходять перевірку огляду на поганий очищення, тоді як нормальний ультрафільтрований концентрат завжди повинен випадати в осад. Деякі виробники дають інше пояснення. Для денатурації серйозне має значення заряд білка. Якщо заряд молекул високий, то білок стійкий до нагрівання (відбувається взаємовідштовхування молекул), що ми і спостерігаємо в деяких випадках. Навіть якщо структура білка і змінюється від температури , то осад не випадає.
Відомий приклад: молоко можна кип'ятити і воно не згортається саме через сильний негативного заряду молочного альбуміну, казеїн в молоці знаходиться у вигляді попередника казеїногену і теж добре розчинний. При скисанні молока кислоти нейтралізують заряд білків, і молоко створоджується.
Типи протеїнів:
Список використаної літератури
| Продукт | Вміст білка, % | Продукт | Вміст білка, % |
| М'ясо | 18-22 | Гречана крупа | 11 |
| Риба | 17-22 | Пшоно | 10 |
| Сир | 20-36 | Горіхи лісові | 12 |
| Яйця | 13 | Горіхи кедрові | 4 |
| Молоко | 3,5 | Картопля | 1,5-2 |
| Хліб житній | 7,8 | Капуста | 1,1-1,6 |
| Рис | 8 | Морква | 0,8-1,6 |
| Горох | 26 | Буряк | 1,6 |
| Соя | 35 | Яблука | 0,3-0,4 |
| Макарони | 9-13 | Вишня | 1-1,1 |
Перевірка на справжність
Широко поширений простий спосіб перевірки білка на справжність шляхом додавання до нього окропу, іноді з подальшим кип'ятінням , внаслідок чого спостерігається процес денатурації з утворенням характерних пластівців і випаданням осаду. Для посилення реакції бажано додати кілька крапель оцту, щоб знизити pH розчину і нейтралізувати негативний заряд.
Деякі продукти не проходять перевірку огляду на поганий очищення, тоді як нормальний ультрафільтрований концентрат завжди повинен випадати в осад. Деякі виробники дають інше пояснення. Для денатурації серйозне має значення заряд білка. Якщо заряд молекул високий, то білок стійкий до нагрівання (відбувається взаємовідштовхування молекул), що ми і спостерігаємо в деяких випадках. Навіть якщо структура білка і змінюється від температури , то осад не випадає.
Відомий приклад: молоко можна кип'ятити і воно не згортається саме через сильний негативного заряду молочного альбуміну, казеїн в молоці знаходиться у вигляді попередника казеїногену і теж добре розчинний. При скисанні молока кислоти нейтралізують заряд білків, і молоко створоджується.
Типи протеїнів:
- Сироваткові протеїни
- Казеїнові протеїни
- Соєві протеїни
- Багатоскладові протеїни
- Яєчний протеїн
- Ізолят - протеїн високого ступеня обробки.
- Гідролізат - практично розщеплений білок, можна сказати, вже амінокислота.
Список використаної літератури
- Аминокислоты в живом организме С.Н. Гараева, Г.В. Редкозубова, Г.В. Постолати, 2009. - 552 с.: ил. ISBN 978-9975-62-269-1 (с. 10 - 12)
- Кретович В. Л. Биохимия растений: Учеб. - 2-е изд., и доп.; для биол. спец. ун-тов. - М.: Высш. шк., 1986. - 503 с., ил. (с. 54 - 56)
- Березов Т. Т., Коровкин Б. Ф. Биологическая химия: Учебник.– 3-е изд., перераб. и доп.– М.: Медицина, 1998.– 704 с.: ил.– (Учеб. лит. Для студентов мед. вузов). ISBN 5-225-02709-1 (с. 417 - 418)