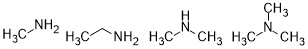
Метиламин, этиламин, диметиламин, триметиламин.
"Прародитель" всех аминов - аммиак NH3 даже не считается органическим соединением, но по свойствам амины похожи на аммиак. Дело в наличии неподелённой электронной пары у азота, благодаря чему он может образовывать четвёртую связь (по донорно-ацепторному механизму), присоединяя к себе протон. Раз амины являются акцепторами протонов, то они выступают и как основания: при растворении в воде вследствие гидролиза дают ионы OH-, то есть создают щелочную среду, а с кислотами реагируют, образуя твёрдые белые кристаллические вещества - соли аминов.
Как видно из структур, амины можно поделить на первичные, вторичные и третичные - по количеству связей азота с углеродом. Наиболее сильно основные свойства выражены у вторичных аминов (таких, как диметиламин).
Простейшие амины (метиламин, этиламин и диметиламин и триметиламин) - газы, легко растворимые в воде. Хорошо растворяется в воде и аммиак - на этом основана известная демонстрация "аммиачный фонтан". Более тяжёлые амины хуже растворяются в воде, но при добавлении кислоты образуют соли и переходят в раствор.
Все амины имеют неприятный запах, который похож на запах аммиака, а ещё напоминает запах несвежей рыбы. Это связано с тем, что при гниении из аминокислот образуются амины, в том числе кадаверин и путресцин ("Cadaver" (лат) - труп, "puter" (лат) - гнилой). Однако эти и похожие амины встречаются даже в здоровом организме и участвуют в важных клеточных процессах.
Нельзя обойти стороной и сами аминокислоты, являющиеся компонентами белков. Это соединения, имеющие в свой структуре как карбоксильный, так и аминный фрагменты, поэтому способные проявлять свойства и кислот, и оснований. В белках почти исключительно встречаются альфа-аминокислоты, примеры которых представлены на рисунке:
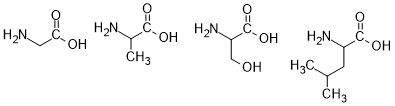
Глицин, аланин, лейцин, серин.
Аминокислоты конденсируются друг с другом, образуя амидную (пептидную) связь. Если число аминокислот невелико (меньше 10), то получающиеся небольшие (по биологическим меркам) соединения называются пептидами. Но зачастую это количество измеряется сотнями или даже тысячами. Те белки, которые мы поглощаем с пищей, распадаются в желудке обратно на составные аминокислоты. В этом участвуют специальные ферменты, которые - та-дам! - также являются белками.
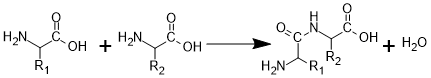
Образование пептидной связи
Амиды являются производными аминов и часто встречаются в лаборатории: например, уже упоминавшийся ранее диметилформамид является очень распространённым растворителем, наряду с N-метилпирролидоном. В отличие от аминов, амиды не проявляют основных свойств.
Важным представителем амидов является нейлон и арамид, выпускающиеся десятками тысяч тонн ежегодно и являющимися полиамидами. Нейлон отличается высокой прочностью, а арамид ("Кевлар" - разновидность арамида) отличается устойчивостью к высоким температурам. Также амидам родственен каптон, хотя он, сторого говоря, относится к полиимидам. Кератин, из которого состоят ногти, волосы, рога крупных животных, а также фиброин, образующий шёлк - все они обладают своими свойствами благодаря прочности пептидной связи.
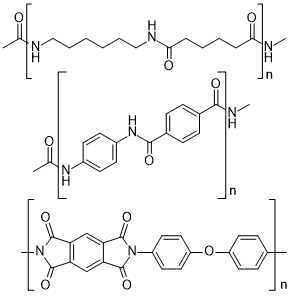
Нейлон, арамид, каптон
Среди аминов много важных соединений: большинство биологически активных соединений, нейротрансмиттеров, лекарств содержат в своей структуре хотя бы одну аминогруппу. Существует отдельный класс соединений, называемый алкалоидами - это вещества растительного происхождения, обладающие основными свойствами (дословно - "подобные щелочам"). Именно аминогруппа придаёт алкалоидам основные свойства. К алкалоидам относятся, например, никотин, эфедрин, хинин, стрихнин.
Амины в непротонированной форме (т.н. "основания" аминов, в противопоставление их солям) обладают не только основными, но и нуклеофильными свойствами: они присоединяют к себе атом углерода, который до этого был связан с активирующей группой - галогеном (хлором, бромом, иодом), кислородом (пример - образование амидов из карбоновых кислот; со спиртами реакция идёт только в жёстких условиях) или любой другой (активирующих групп много, и это тема отдельной статьи). Третичные амины - исключение: новому заместителю уже некуда встать, но при определённых условиях азот всё-таки может образовывать четвёртую связь по донорно-акцепторному механизму, образуя т.н. четвертичные аммониевые соли.
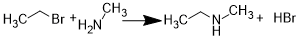
Реакция аминов с галогеналканами (реакция нуклеофильного замещения) на примере бромэтана и метиламина.
Это очень важное свойство аминов, и оно позволяет чаще всего без труда получать амины с нужными заместителями: из первичных - вторичные, из вторичных - третичные. Образующаяся кислота (в данном случае - бромоводородная), связываясь с аминами, будет мешать протеканию реакции, поэтому обязательно присутствие более сильного основания - например, поташа или даже щёлочи.
Также амины реагируют с уже известными нам альдегидами и кетонами, образуя имины. Это соединения с двойной связью C-N - неустойчивые соединения, которые находятся в равновесии с исходными веществами.
Аммиачный фонтан https://www.youtube.com/watch?v=e_VDiLlmyFE
Кадаверин https://ru.wikipedia.org/wiki/Кадаверин
Каптон (англ.) http://www.dupont.com/products-and-services/membranes-films/polyimide-films/brands/kapton-polyimide-film.html
Кевлар: материал прочнее стали http://www.popmech.ru/history/5383-spasitel-zhizney-kevlar-prochnee-stali/
