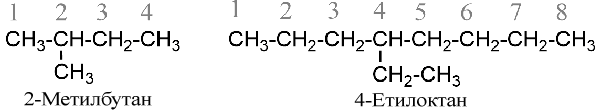Алканы образуют гомологический ряд, в котором каждый член отличается на постоянную структурную единицу -CH2-, что называется гомологической разностью. Простейший представитель - метан CH4.
- Общая формула алканов: CnH2n+2
Содержание статьи:
Изомерия
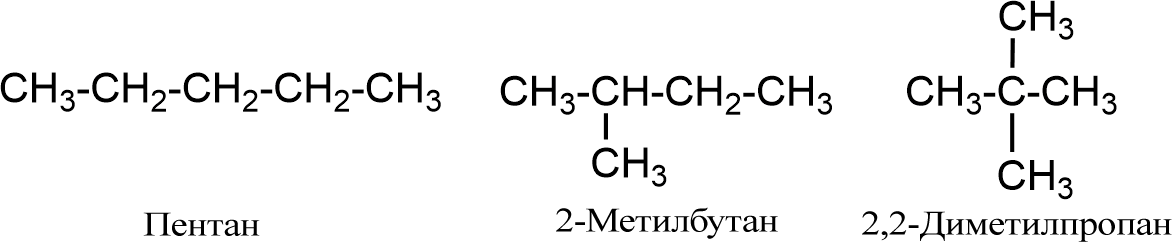
Начиная с бутана C4H10 для алканов характерна структурная изомерия. Количество структурных изомеров возрастает с увеличением числа углеродных атомов в молекуле алканов. Так, для пентана C5H12 известно три изомеры, для октана C8H18 - 18, для декана C10H22 - 75.
Для алканов кроме структурной существует конформационная изомерия и начиная с гептана - енантіомерія:
Номенклатура IUPAC
В названиях алканов используют префиксы н-, втор-, изо, трет-, нео:
- н- означает нормальную (нерозгалужену) строение углеводородного цепи;
- втор- применяется только для вторичного бутила;
- трет- означает алкил третичной структуры;
- изо разветвления на конце цепи;
- нео используется для алкілу с четвертичным атомом углерода.
Номенклатура разветвленных алканов построена основана на следующих основных правилах:
- Для построения названия выбирают длинную цепь атомов углерода и нумеруют его арабскими цифрами (локантами), начиная с конца, ближе к которому находится заместитель, например:
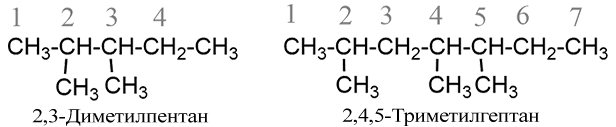
- Если одна и та же алкільна группа встречается более одного раза, то в названии перед ней ставят помножуючі приставки ди- (перед гласной ди-), три-, тетра- и т. п. и обозначают цифрой каждый алкил отдельно, например:
Необходимо заметить, что для сложных остатков (групп) применяются помножуючі префиксы вроде бис-, трис-, тетракіс- прочее.
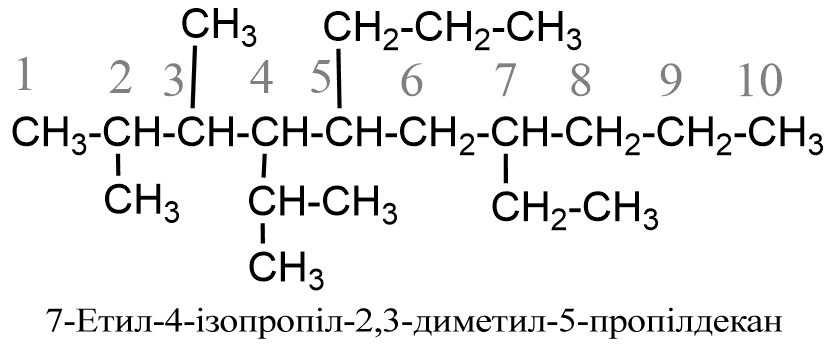
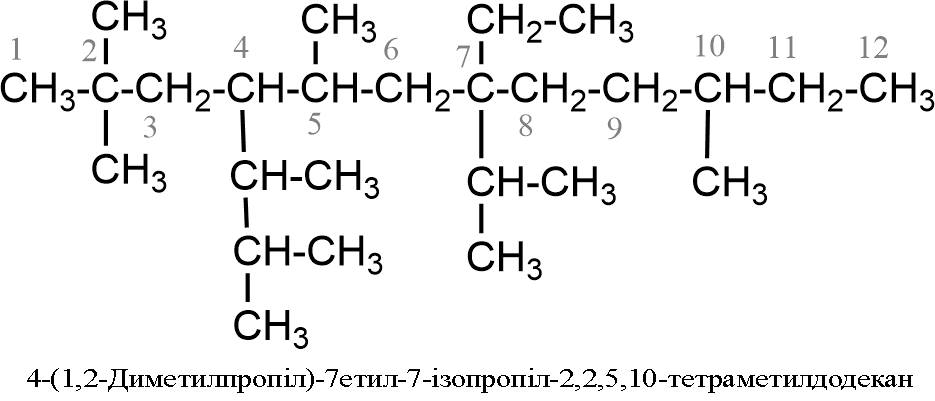
- Если в боковых ответвлениях главной цепи размещены различные алкіли-заместители, то их переразовують по алфавиту (при этом помножуючі приставки ди-, тетра- и т. п, а также префиксы н-, втор-, трет- не принимают во внимание), например:
- Если возможны два или более вариантов длиннейшей цепи, то выбирают тот, который имеет максимальное количество боковых разветвлений.
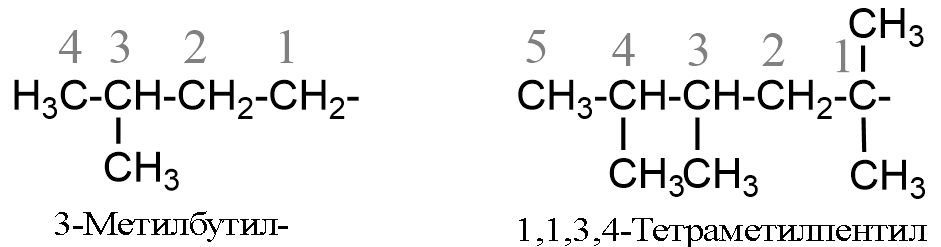
- Названия сложных алкильных групп строятся по тем же принципам, что и названия алканов, но нумерация цепи алкілу всегда автономна и начинается с того атома углерода, имеющего свободную валентность, например:
- При использовании в названии такой группы ее берут в скобки и в алфавитном порядке учитывается первая буква названия всей:
Промышленные методы добычи
1. Извлечения алканов газа. Природный газ состоит главным образом из метана и небольших примесей этана, пропана, бутана. Газ под давлением при пониженных при пониженных температурах разделяют на соответствующие фракции.
2. Извлечения алканов из нефти. Сырую нефть очищают и подвергают переработке (розгонка, фракціювання, крекинг). Из продуктов переработки получают смеси или индивидуальные соединения.
3. Гидрирование угля (метод Ф. Бергіуса, 1925 г.). Каменный или бурый уголь в автоклавах при 30 МПа в присутствии катализаторов (оксиды и сульфиды Fe, Mo, W, Ni) в среде углеводородов гидрированные и превращаются в алканы, так называемое моторное топливо:
nC + (n+1)H2 = CnH2n+2
4. Оксосинтеза алканов (метод Ф. Фишера - Г. Тропша, 1922 г.). По методу Фишера - Тропша алканы получают из синтез-газа. Синтез-газ представляет собой смесь CO и H2 с различным соотношением. Его получают из метана одной из реакций, которые происходят при 800-900°C в присутствии оксида никеля NiO, нанесенного на Al2O3:
CH4 + H2O ⇄ CO + 3H2
CH4 + CO2 ⇄ 2CO + 2H2
2CH4 + O2 ⇄ 2CO + 4H2
Алканы получают по реакции (температура около 300°C, катализатор Fe-Co):
nCO + (2n+1)H2 → CnH2n+2 + nH2O
Образованная смесь углеводородов, состоящая в основном из алканов строения (n=12-18), называют "синтином".
5. Сухая перегонка. В относительно небольших количествах алканы получают при помощи сухой перегонки или нагрева угля, сланцев, древесины, торфа без доступа воздуха. Примерный состав полученной смеси при этом составляет 60% водорода, 25% метана и 3-5% этилена.
Лабораторные методы добывания
1. Получение из галогеналкілів
1.2 Взаимодействие с літійдіалкілкупратами. Метод (иногда называют реакцией Е. Коре - Х. Хауса) заключается во взаимодействии реакционноспособных літійдіалкілкупратів R2CuLi с галогеналкілами. Сначала происходит взаимодействие металлического лития с галогеналканом в среде эфира. Далее соответствующий алкіллітій реагирует с галогенідом меди(I) с образованием растворимого літійдіалкілкупрату:
1.3 Восстановление галогеналкілів. Восстанавливать галогеналкіли возможно каталитически возбужденным молекулярным водородом, атомарным водородом, йодоводнем тому подобное:
5. Сухая перегонка. В относительно небольших количествах алканы получают при помощи сухой перегонки или нагрева угля, сланцев, древесины, торфа без доступа воздуха. Примерный состав полученной смеси при этом составляет 60% водорода, 25% метана и 3-5% этилена.
Лабораторные методы добывания
1. Получение из галогеналкілів
1.1. Взаимодействие с металлическим натрием (Вурц, 1855 г.). Реакция состоит во взаимодействии щелочного металла с галогеналкілом и применяется для синтеза высших симметричных алканов:
2CH3-I + 2Na ⇄ CH3-CH3 + 2NaI
В случае участия в реакции двух разных галогеналкілів образуется смесь алканов:
3CH3-I + 3CH3CH2-I + 6Na → CH3-CH3 + CH3CH2CH3 + CH3CH2CH2CH3 + 6NaI
CH3Cl + 2Li → CH3Li + LiCl
2CH3Li + CuI → (CH3)2CuLi + LiI
При взаимодействии такого літійдіалкілкупрату с соответствующим галогеналкілом образуется конечное соединение:
(CH3)2CuLi + 2CH3(CH2)6CH2-I → 2CH3(CH2)6CH2-CH3 + LiI + CuI
Метод позволяет достичь выхода алканов почти 100% при применении первичных галогеналкілів. При их вторичной или третичной строении выход составляет 30-55%. Природа алкільної составляющей в літійдіалкілкупраті мало влияет на выход алкану.
1.3 Восстановление галогеналкілів. Восстанавливать галогеналкіли возможно каталитически возбужденным молекулярным водородом, атомарным водородом, йодоводнем тому подобное:
CH3I + H2 → CH4 + HI (катализатор Pd)
CH3CH2I + 2H → CH3CH3 + HI
CH3I + HI → CH4 + I2
Метод имеет препаративне значение, часто используют сильный восстановитель - йодоводень.
2. Получение из солей карбоновых кислот.
2.1 Электролиз солей (Кольбе, 1849 г.). Реакция Кольбе заключается в электролизе водных растворов солей карбоновых кислот:
2. Получение из солей карбоновых кислот.
2.1 Электролиз солей (Кольбе, 1849 г.). Реакция Кольбе заключается в электролизе водных растворов солей карбоновых кислот:
R-COONa ⇄ R-COO- + Na+
На аноде анион карбоновой кислоты окисляется, образуя свободный радикал, и легко декарбоксилюється или отщеплять CO2. Алкильные радикалы далее вследствие рекомбинации превращаются в алканы:
R-COO- → R-COO• + e-
R-COO• → R• + CO2
R• + R• → R-R
Препаративный метод Кольбе считается эффективным при наличии соответствующих карбоновых кислот и невозможности применить другие методы синтеза.
2.2 Сплавления солей карбоновых кислот со щелочью. Соли щелочных металлов карбоновых кислот при славленні с щелочью образуют алканы:
CH3CH2COONa + NaOH → Na2CO3 + CH3CH3
3. Восстановление кислородсодержащих соединений (спиртов, кетонов, карбоновых кислот). Восстановителями выступают вышеупомянутые соединения. Чаще всего применяют йодоводень, который способен восстанавливать даже кетоны:
R-OH + 2HI → R-H + I2 + H2O
CH3-CO-CH3 + 4HI → CH3-CH2-CH2 + 2I2 + H2O
В препаративному плане часто используют восстановление карбонильных соединений Е. Клемменсеном и М. Кіжнером.
4. Гидрирование ненасыщенных углеводородов. Реакция гидрирования ненасыщенных соединений широко применяется при переходе от одного класса углеводородов к другому:
4. Гидрирование ненасыщенных углеводородов. Реакция гидрирования ненасыщенных соединений широко применяется при переходе от одного класса углеводородов к другому:
CH3-CH=CH2 + H2 → CH3-CH2-CH3 (катализатор Pt, Ni)
CH≡CH + 2H2 → CH3-CH3 (катализатор Pt, Ni)
Реакции гидрирования показывают генетическую связь между насыщенными и ненасыщенными соединениями и возможность их взаимного перехода друг в другие.
Физические свойства
Первые четыре представителя алканов от метана до бутана (C1-C4) - газы, от пентана до пентадекану (C5-C15 - жидкости, от гексадекану (C16) - твердые вещества. Увеличения их молекулярных масс приводит к увеличению температур кипения и плавления, при чем алканы с разветвленной цепью кипят при более низкой температуре, чем алканы нормального строения. Это объясняется меньшей вандерваальсівською взаимодействием между молекулами разветвленных углеводородов в жидком состоянии. Температура плавления четных гомологов выше по сравнению с температурой соответственно для нечетных.
Алканы гораздо легче за воду, неполярные и трудно поляризуются, однако растворимы в большинстве неполярных растворителей, благодаря чему сами могут быть растворителем для многих органических соединений.